Treiber und Funktionen von Blatt-assoziierten Endophyten-Gemeinschaften
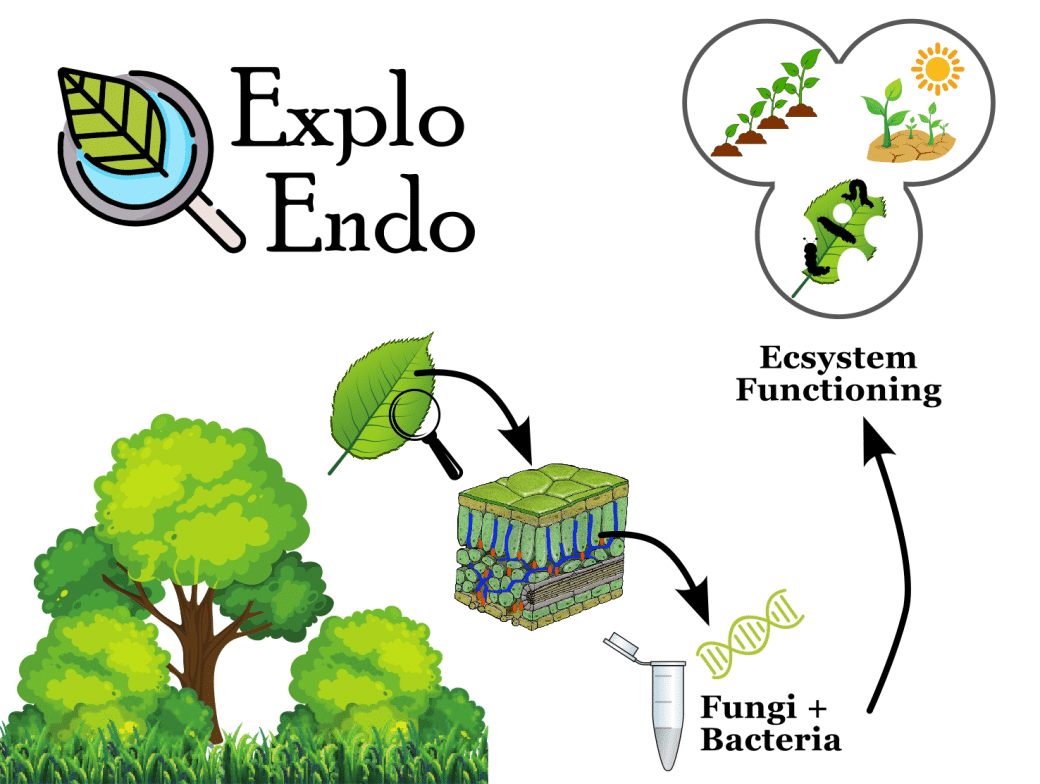
Als blatt-assoziierte Endophyten werden mikroskopische Pilze und Bakterien bezeichnet, die das Blattgewebe von Pflanzen besiedeln, ohne offensichtliche Schäden zu verursachen. Stattdessen können blatt-assoziierte Endophyten auch das Pflanzenwachstum und den Nährstoffkreislauf anregen und die Pflanze gegen Trockenstress, Krankheitserreger und Herbivoren schützen. Trotz steigender Anzahl an Publikationen, bestehen noch grundlegende Verständnislücken, z.B. zur Verbreitung, Diversität, den Treibern und den Funktionen von Blatt-assoziierten Endophyten, insbesondere auch im Hinblick auf möglicherweise interaktive Effekte von steigender Landnutzungsintensität und sinkender Pflanzendiversität.
Wir werden die Diversität, Treiber und ökologischen Zusammenhänge von Blatt-assoziierten Endophyten-Gemeinschaften mit zwei Ansätzen zu untersuchen:
- (1) wirtspflanzenspezifische Analysen zu den Endophyten-Gemeinschaften in 15 typischen Wald- und Grünlandarten,
- (2) Umwelt-DNA-Analysen getrockneter Grünland Biomasseproben von 2018–2025.
(H1) Innerhalb der untersuchten Zielpflanzenarten steigt die Diversität Blatt-assoziierter Endophyten mit steigender der Diversität der umgebenen Pflanzen-Gemeinschaft, steigender Diversität der umgebenden Lebensraumtypen, und sinkt mit zunehmender Landnutzungsintensität.
(H2) Durch ihre Unterschiede im Artenreichtum und der physischen Struktur erwarten wir, dass die Zusammenhänge von Endophyten- und Pflanzendiversität sich zwischen Wald- und Grünlandflächen unterscheiden.
(H3) In den Umwelt-DNA-Proben erwarten wir, dass eine niedrigere Pflanzendiversität, eine höhere Landnutzungsintensität, und erhöhter Trockenstress zu einer erhöhten jährlichen Schwankung in den Gemeinschaften der Blatt-assoziierten Pilze führt.
Für die Analyse der Ziel-Pflenzenarten werden wir Blattproben in allen experimentellen Grünland- und Waldflächen für die folgenden häufigen Pflanzenarten sammeln:
(1) Fagus sylvatica L., (2) Acer pseudoplatanus L., (3) Picea abies (L.) H. Karst., (4) Pinus sylvestris L., (5) Milium effusum L., (6) Carex sylvatica Huds., (7) Anemone nemorosa L., (8) Urtica dioica L., (9) Poa trivialis L., (10) Dactylis glomerata L., (11) Cerastium holosteoides Baumg., (12) Trifolium repens L., (13) Veronica chamaedrys L., (14) Plantago lanceolata L., (15) Alopecurus pratensis L.
Alle Blattproben werden auf Eis gelagert und in die Labore der Martin-Luther-Universität Halle-Wittenberg transportiert, wo wir zuerst ihre Oberfläche sterilisieren und die Proben dann homogenisieren.
Für den Umwelt-DNA-Ansatz werden wir mit dem Kernprojekt 5 (Pflanzendiversität) kooperieren, um die schon gesammelten, getrocknete und homogenisierte Proben der oberirdischen Grünland-Biomasse aus den Jahren 2018–2025 zu analysieren.
Aus allen Blatt- und Biomasseproben werden wir zuerst die DNA mithilfe eines gDNA Plant Kits (Invitrogen™, ChargeSwitch®, Thermo Fisher, München, Deutschland) extrahieren und dann interne transkribierte Spacer-1-Genregion für Pilze (unter Verwendung der Primer ITS1F und ITS2) sowie die V4-Region des 16S-rRNA-Gens für Bakterien (unter Verwendung der Primer F515 und R806) amplifizieren. Jeweils 380 äquimolar-gepoolte Mischproben aus Pilz- und Bakterien-DANN (zur Kostenreduktion) werden mittels Illumina sequenziert und die erhaltenen DNA-Sequenzen werden mit einer DADA2-Pipeline verarbeitet und danach zu Pilz- und Bakterien-Amplicon-Sequenzvarianten zugeordnet. Die Verteilung dieser ASVs werden wir dann mit generalisierten, gemischten Modellen, boosted-regression-Modelle und multivariater Methoden analysieren.